Bizonyára a mindennapi életben már hallották, hogy valamit eleminek vagy elemnek neveznek. Minden hétköznapi anyag, beleértve a testünket alkotó szöveteket és csontokat is, ezekből az elemekből épül fel, amelyekből meglepően kevés fajta létezik.
Mitől különbözik az egyik elem a másiktól?
Erre a kérdésre akkor tudunk teljes egészében válaszolni, ha az atomok felépítését behatóbban megismerjük. Az elemek az atomi skálán különböznek egymástól; az arany a magnéziumtól eltérő tulajdonságokkal rendelkezik, mivel az egyedi atomjaik szerkezete más. Ez a különbség meghatározza az elemek fizikai tulajdonságait, például a tiszta formában mutatott külső megjelenésüket (az arany csillogó, kemény, sárga anyag, míg a magnézium ezüstös és jobban alakítható). Azonban még fontosabb, hogy az elemek kémiai tulajdonságait, vagyis azt, hogy hogyan lépnek kölcsönhatásba más anyagokkal (az arany nagyon ellenálló, míg a magnézium könnyen reagál a vízzel), is az atomi szerkezet szabja meg. Továbbá ez a szerkezet felelős azért is, hogy egy adott elem milyen másik elemekkel kombinálódhat, azaz alkothat összetett anyagot.
Az elemeket atomi szerkezetük, tehát tulajdonságaik alapján egy nagyon hasznos eszköz, a periódusos rendszer segítségével rendszerezzük, amelyet majd a későbbiekben részletesebben is ismertetünk.
A minket körülvevő világot alkotó elemeket nem lehet mesterségesen előállítani, az valahogyan természetes úton jött létre. Vajon honnan származik a testünk építőkövének számító szén? Bármilyen meglepő, a Földön található minden stabil elem valahol messze, az űrben jött létre. A könnyű elemek a vasig bezárólag a csillagok belsejében az úgynevezett nukleoszintézis során alakultak ki. A többi elem pedig a csillagok halálakor bekövetkező kataklizmatikus, hatalmas robbanásokban, a szupernóvákban formálódott. Mindkét folyamatot a későbbiekben részletesen tárgyalunk. Azonban már most is megérthetjük, hogy azért van az aranynál több szén a világegyetemben, mert csak a nagyon nagy tömegű csillagok válnak szupernóvává és képesek a nehéz elemek előállítására ezáltal.
Az atomok létezését már az ókori görögök is felvetették, amikor Démokritosz felismerte, hogy egy ponton túl már nem tudja kisebb darabokra szelni a kenyerét; oszthatatlanná vált. Démokritosz arra jutott, hogy minden valamilyen alapvető darabokból van összerakva, amelyeket nem lehet megsemmisíteni. Ezeket a darabokat a görögül "atomos"-nak, azaz szétvághatatlannak nevezte.
Azonban az atomok modernebb elképzelése a kémia kialakulásával köthető össze. John Dalton vette észre, hogy 8 gramm oxigén mindig pontosan 1 gramm hidrogénnel elegyedik. Ez vezetett ahhoz az elmélethez, hogy egy elemnek adott számú, valamilyen kisméretű alkotórésze egy másik elemnek csak bizonyos számú kisméretű alkotórészéhez kapcsolódhat. Ennek a segítségével jutottak el az atomok fogalmának bevezetéséhez. Ugyan a vegyészek ismerték fel az atomokat, de a fizikusok jöttek rá arra, hogy az atomokban jóval több rejlik, mint ahogyan azt először gondolták.
Az atommag felfedezése
Amikor elfogadottá vált, hogy kis méreteknél az anyag építőköveinek az atomokat tekinthetjük, a kutatók elkezdték koherens elméletbe foglalni azt, hogy mi határozza meg egy atom tulajdonságait, és miért viselkedik egy aranyatom másként, mint egy magnéziumatom. A leginkább elfogadott elképzeléssé a "mazsolás sütemény modell" vált. Ennek értelmében az atom nem más, mint pozitív töltések tengere, amelybe elszórva negatív töltések merülnek, és ezek a töltések kiegyenlítik egymást úgy, hogy kifelé az atom semleges jelleget mutat.
Arra, hogy az atomok valódi szerkezete teljesen másmilyen 1911-ben Rutherford kísérlete mutatott rá. Igen vékony (néhány atomnyi vastagságú) aranyfóliát bombázott az akkoriban felfedezett alfa-részecskékkel (pozitív töltésű részecskék, amelyekről ma már tudjuk, hogy héliumatommagok). Azt találta, hogy ellentétben a várakozásokkal, a részecskék nagyon kis hányada szóródott visszafelé, a legtöbbjük kis szögben térült csak el vagy egyenesen áthaladt a fólián. Ebből Rutherford arra következtetett, hogy az atomok valójában egy nagyon kis térfogatú pozitív töltésű központtal rendelkeznek, amellyel történő frontális ütközésben pattannak vissza az alfa-részecskék. Továbbá azt is kijelenthette, hogy az atomok nagyrészt üres térből állnak, amelyen a részecskék akadály nélkül át tudnak hatolni. A kis szögben szóródott alfa-részecskék pedig olyanok, amelyek a pozitív töltésű maghoz közel haladtak és az azonos töltések taszítása miatt térültek el.
Végső modellje az atom középpontjában elhelyezkedő, pozitív töltésű, kicsiny labdából, amelyet az atom magjának tekintett, illetve a mag körül keringő (a bolygókhoz hasonlóan), annak töltését kiegyensúlyozó, negatív töltésű elektronokból állt. Mindaddig Rutherford modellje volt az elfogadott, amíg még modernebb kvantumfizikai kísérletek arra utaltak, hogy ez a modell sem teljesen helytálló.
Az atommag
Ahogy az elnevézésük is ezt fejezi ki, a magfizikusok az atom magjának vislkedésére összpontosítanak, ezért szerkezetének megismerése kulcsfontosságú számukra. Az elektronokat J.J. Thompson fedezte fel, amikor megmutatta, hogy az akkoriban katódsugárzásnak nevezett jelenség nem más, mint negatív töltésű töltött részecskék összessége. Ezen részecskék töltés/tömeg arányát Millikan mérte meg töltött olajcseppek segítségével. Már sok évvel Rutherford kísérlete előtt többen indítványozták, hogy minden atom hidrogénatomokból épül fel, ami majdnem helyes is. 1917-ben Rutherford újabb kísérletet végzett, amelyben alfa-részecskékkel bombázott nitrogén gázt. Az alkalmazott detektor olyan jeleket rögzített, amelyeket hidrogénatomok által keltettnek azonosított, amiből arra következtetett, hogy a nitrogénatommagok az alfa-részecskékkel történt ütközés hatására hidrogénatommagot bocsátottak ki. Rutherford számára ez azt jelentette, hogy a nitrogénatommag hidrogénatommagot, vagyis protont tartalmaz. Ez volt az első kísérlet, amelyben valaki mesterséges magreakciót hozott létre, és azt be is bizonyította.
Ezen a ponton vezették be a kutatók a tömegszám és a rendszám fogalmát.
A tömegszám az atom tényleges tömege (tulajdonképpen azt is mondhatjuk, hogy az atommag tömege, mivel az elektronok hozzájárulása elhanyagolható), míg a rendszám az atomban lévő protonok, illetve az elektronok számával egyenlő. A neutronok létezését elsőként Rutherford javasolta 1920-ban, amikor az atommagok rendszáma és tömegszáma közötti rendellenességre keresett magyarázatot. Azonban James Chadwick volt az első, aki 1932-ben megmutatta, hogy a korábban gamma-sugárzásnak gondolt jelenséget egy új, semleges részecske bevezetésével lehet megmagyarázni, amelynek tömege a protonéval nagyjából megegyezik. A sugárzást alkotó részecskéket neutronoknak nevezték el, és tömegük pontosan olyan volt, amivel a rendszám és tömegszám közötti rendellenességet fel lehetett oldani.
Az atommagban lévő protonok és neutronok közös neve nukleon. Őket az erős kölcsönhatás tartja össze, amely az ismert négy alapvető kölcsönhatás egyike. Ez a kölcsönhatás 1038-szor erősebb, mint a gravitáció, hatótávolsága csak 10-15m, de messze meghaladja a protonok azonos töltése között fellépő elektromos taszítást.
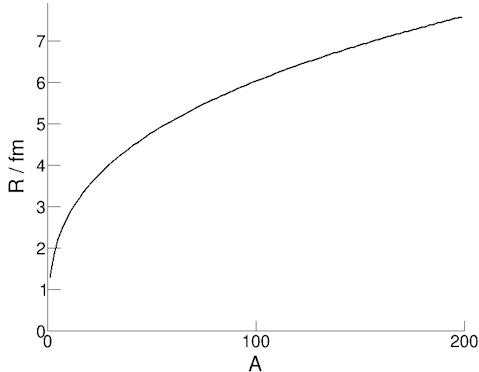
Az atommagok sugarát meghatározhatjuk, ha elektronoknak az atommagokon történő szórásának mintázatát vizsgáljuk. A lendületmegmaradás törvényét felhasználva számolásokat is végezhetünk, és a kísérletek azt mutatják, hogy a sugár az alábbi összefüggéssel írható le:
R = r0 A1/3
ahol R az atommag sugara, A a nukleonok száma és r0 egy állandó (a nukleon sugara), melynek értéke ≈ 1,3fm.